全身型重症筋無力症患者へのソリリス®投与における質問集(FAQ)
ソリリス®投与に関するよくある質問をまとめました
投与方法
- ソリリス®はどんな患者さんに投与すればよいですか?
- 抗AChR抗体を測定せずに投与してもよいですか?
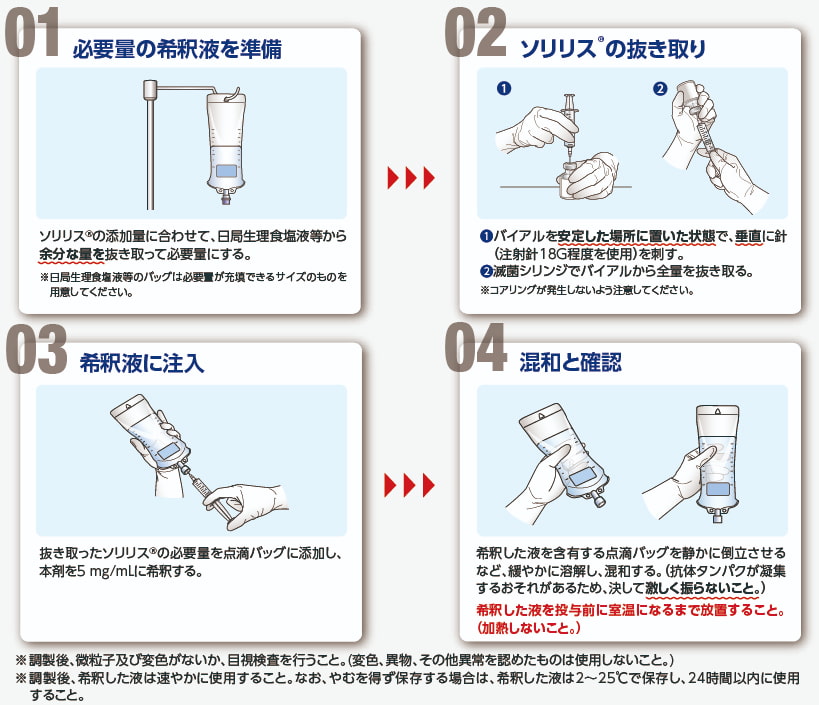
- ソリリス®はどのように投与・調製すればよいですか?
- 髄膜炎菌ワクチンの接種を行わずにソリリス®の投与は可能ですか?
- 成人において他のMG治療薬(抗コリンエステラーゼ薬、経口ステロイド薬、カルシニューリン阻害薬、IVIg、エフガルチギモド アルファ)とソリリス®は併用してもよいですか?
-
成人において他のMG治療薬とソリリス®の併用は可能です。全身型MGに対するソリリス®の臨床試験(C08-001試験、REGAIN試験、REGAIN継続試験)は、全患者が試験期間中に併用薬を使用していました1-5)。 しかしながら、全身型MG患者に対し、人免疫グロブリン製剤又はエフガルチギモド アルファとの併用投与によって、本剤の血清中濃度が低下することがあります。 人免疫グロブリン製剤又はエフガルチギモド アルファと本剤を併用する場合には、患者の状態を十分に観察してください。
<併用注意 (併用に注意すること)>
薬剤名等 臨床症状・措置方法 機序・危険因子 人免疫グロブリン製剤 (ポリエチレングリコール処理人免疫グロブリン等) 人免疫グロブリン製剤との併用投与によって本剤の効果が減弱するおそれがあるので、併用する場合には、本剤の補充投与を考慮すること。 人免疫グロブリン製剤との継続的な併用投与により、本剤の血清中濃度が低下する可能性がある6-8)。 エフガルチギモド アルファ(遺伝子組換え) 本剤の効果が減弱するおそれがあるので、本剤による治療を開始する場合には、エフガルチギモド アルファのサイクル投与における最終投与から2週間後以降に投与することが望ましい。 エフガルチギモド アルファにより、本剤を含む胎児性Fc受容体(FcRn)に結合する薬剤の血清中濃度が低下する可能性がある。 本邦では一部のIVIgにはMGの適応はありません。
引用 1)社内資料:海外第Ⅱ相臨床試験(C08-001)(承認時評価資料) 2)社内資料:第Ⅲ相プラセボ対照二重盲検比較臨床試験(ECU-MG-301)(承認時評価資料) 3)Howard JF Jr, et al. Lancet Neurol 2017; 16: 976-986. [利益相反:本試験はAlexion Pharmaceuticals, Inc.の支援のもと実施されました] 4)社内資料:第Ⅲ相ECU-MG-301継続試験(ECU-MG-302)(承認時評価資料) 5)Muppidi S, et al. Muscle Nerve 2019; 60: 14-24. [利益相反:本試験はAlexion Pharmaceuticals, Inc.の支援のもと実施されました] 6)Jin F, et al. Hum Immunol 2005; 66: 403-410. 7)Wang W, et al. Clin Pharmacol Ther 2008; 84: 548-558. 8)Fitzpatrick AM, et al. J Peripher Nerv Syst 2011; 16: 84-91.
関連する質問
電話でのお問い合わせ
フリーダイヤル 0120-577-657
受付時間 9:00 ~ 17:30(土、日、祝日及び当社休業日を除く)
- ソリリス®投与中に血液浄化療法を行った場合、投与量の調整は必要ですか?
-
血液浄化療法(透析を除く)によりソリリス®の一部が除去されることから、MG患者さんへのソリリス®投与中に血液浄化療法を施行する必要がある場合は、下表を参考にソリリス®の補充投与を考慮してください。なお。下表はシミュレーション結果に基づいて設定されたものですので、補充投与後は患者の状態を慎重に観察してください。
直近の本剤投与量 本剤の補充用量 補充投与の時期 血液浄化療法 300mg 1回につき300mg 施行後60分以内 600mg以上 1回につき600mg 関連する質問
電話でのお問い合わせ
フリーダイヤル 0120-577-657
受付時間 9:00 ~ 17:30(土、日、祝日及び当社休業日を除く)
- ソリリス®投与中に免疫グロブリン大量静注療法を行った場合、投与量の調整は必要ですか?
-
免疫グロブリン大量静注療法によりエンドソーム内の胎児性Fc受容体(FcRn)のリサイクリング機能が阻害される可能性があることから、MG患者さんへのソリリス®投与中に免疫グロブリン大量静注療法を施行する必要がある場合は、下表を参考にソリリス®の補充投与を考慮してください。なお。下表はシミュレーション結果に基づいて設定されたものですので、補充投与後は患者の状態を慎重に観察してください。
直近の本剤投与量 本剤の補充用量 補充投与の時期 免疫グロブリン
大量静注療法600mg以下 1回につき300mg 施行直後 900mg以上 1回につき600mg 本邦では一部のIVIgにはMGの適応はありません。
関連する質問
電話でのお問い合わせ
フリーダイヤル 0120-577-657
受付時間 9:00 ~ 17:30(土、日、祝日及び当社休業日を除く)
- ソリリス®投与はいつまで続ければよいですか?
-
基本的にソリリス®は根治をする薬剤ではないため、リスクベネフィットを考慮し、投与継続の必要性をご判断ください。 なお、ソリリス®の全身型MG患者を対象とした臨床試験では、ほとんどの治療反応例で投与開始後12週までに症状の改善が得られていました。全身型MG患者で他の免疫抑制剤を併用している患者さんにおいては、髄膜炎菌感染症のリスクが高い可能性があることから、リスクベネフィットを考慮し、投与開始後12 週までに症状の改善が認められない患者さんでは、ソリリス®の投与中止を検討してください。
関連する質問
電話でのお問い合わせ
フリーダイヤル 0120-577-657
受付時間 9:00 ~ 17:30(土、日、祝日及び当社休業日を除く)
- ソリリス®を投与される患者さん及びそのご家族にはどのような説明をすればよいですか?
-
患者さん及びそのご家族には、「ソリリス®の効果」、「ソリリス®を使う前に確認すべきこと」、「ソリリス®の投与方法」、「ソリリス®投与中に気をつけなければならないこと」、「起こり得る副作用と主な症状」などを説明します。 特に注意喚起する必要があるのは、ソリリス®投与により、髄膜炎菌感染症、肺炎球菌感染症、インフルエンザ菌b型感染症などに罹患しやすくなることです。特に、髄膜炎菌感染症が発症した場合には急激に重症化し死亡に至ることがあります。 このため、本剤投与中の患者さん及びそのご家族に対しては、重篤な感染症に罹患する可能性及びそれに関連する以下の徴候、症状について説明し、患者さん及びそのご家族の意識を高めてください。
<髄膜炎菌感染症が疑われる注意が必要な症状> 初期症状は、以下のような一般的な風邪やインフルエンザの症状と区別がつきにくい場合があるので注意が必要です。 ・発熱 ・頭痛 ・吐き気、嘔吐 ・筋肉の痛み その他、髄膜炎菌感染症には以下のような症状があります。 ・錯乱(混乱して考えがまとまらない、物事を理解できない) ・うなじのこわばり(首の後ろが硬直しあごを傾けられない) ・発疹、出血性皮疹(赤や紫色の斑点状の発疹) ・光に対する過剰な感覚(光が異様にギラギラ輝いて見える、異常にまぶしく感じる等) ・手足の痛み
乳幼児においては、上記以外に下記の症状にも注意が必要です。 ・手足が冷たい ・顔色が悪い ・眠気、低緊張、無反応、目覚めにくい ・異常な泣き方、うめき、怒りっぽい ・触られるのを嫌がる ・抑えられない震え ・授乳/食事を嫌がる ・頭部のこわばり/膨らみ(通常軟らかい部分) ・呼吸促迫、呼吸困難
また、本剤投与中の患者さん及びそのご家族に患者安全性カードを渡して、常に携帯する必要があること、受診した医療従事者に提示する必要があることを説明してください。患者さん及びそのご家族には、患者安全性カードに記載の「髄膜炎菌感染症が疑われる注意が必要な症状」(上記)のいずれかを認めた場合や感染症にかかったかもしれないと思ったら、直ちに担当医師の診察を受けるよう指導してください。 なお、担当医師と連絡が取れない場合にはすぐに救急車を呼び、患者安全性カードを救急救命室のスタッフに提示するよう指導してください。
関連する質問
電話でのお問い合わせ
フリーダイヤル 0120-577-657
受付時間 9:00 ~ 17:30(土、日、祝日及び当社休業日を除く)